Approches thérapeutiques
Personnels impliqués: Séverine Bégard, David Blum, Luc Buée, Valérie Buée-Scherrer, Charlotte Branquart, Thierry Burnouf, Raphaëlle Caillierez, Léna Chesnais, Clément Danis, Vincent Deramecourt, Sabiha Eddarkaoui, Emilie Faivre, Giovanni Ferro, Coraille Formentin, Nicolas Geoffre, Marine Hervet, Dimitri Kwiatkowski, Brenda Lammens, Nhi Le, Sarah Leclercq, Thibaud Lebouvier, Simon Lecerf, Evangelia Manousaki, Abinaya Srinivasan, Simon Thiou
Nous développons plusieurs axes thématiques visant à développer de nouvelles modalités thérapeutiques et à fournir des preuves de concept dans des modèles cellulaires et animaux afin de permettre le développement d’essais thérapeutiques chez les patients atteints de la maladie d’Alzheimer et de Tauopathies.
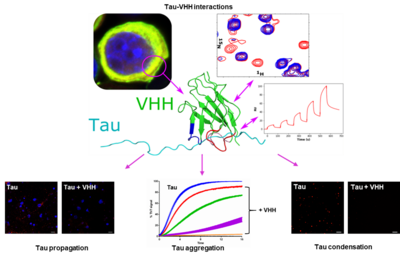
En collaboration avec Isabelle Landrieu (Cnrs, Lille), nous avons sélectionné, caractérisé et optimisé divers ensembles d'anticorps à simple domaine issus des Camelidae, également appelés nanocorps ou VHHs qui ciblent différents épitopes et formes de la protéine Tau. Ces nanocorps ont la particularité d’être dix fois plus petit qu’un anticorps conventionnel et peuvent accéder à des zones cellulaires inaccessibles aux anticorps classiques. Ils représentent une alternative prometteuse aux anticorps monoclonaux classiques, avec un potentiel accru pour le ciblage intracellulaire et une meilleure pénétration tissulaire. Leur développement pourrait aboutir à des traitements plus efficaces et moins invasifs pour les maladies neurodégénératives. Ils sont capables de reconnaître spécifiquement différentes formes de Tau, tant à l’extérieur qu’à l’intérieur des cellules (https://lejournal.cnrs.fr/maladie-alzheimer-demence-neurones-nanocorps).
Cela ouvre la voie à des stratégies thérapeutiques innovantes pour les maladies neurodégénératives comme la maladie d’Alzheimer, où l’accumulation et la propagation de Tau sont impliquées dans la mort neuronale. Nous utilisons ces outils moléculaires pour étudier les différents mécanismes physiopathologiques de Tau tels que la séparation de phase liquide-liquide (condensation), l’agrégation et la propagation. Nous évaluons également le potentiel thérapeutique des nanocorps dans différents modèles reproduisant la pathologie Tau.
Dans ce contexte, nous avons récemment mis au point des nanocorps capables de bloquer l’internalisation de la protéine Tau par les neurones (https://www.insb.cnrs.fr/fr/cnrsinfo/comprendre-alzheimer-des-petits-anticorps-prometteurs). Nous développons également des conjugués de nanocorps capables de cibler Tau dans les cellules vivantes, y compris les neurones, pour moduler sa liaison à ses partenaires et interférer avec son rôle pathologique. Ces travaux pourraient révolutionner la prise en charge des Tauopathies dans les années à venir. En ces sens, nous formons une génération de futurs chercheurs au sein de notre réseau doctoral Européen TAME https://tame-itn.eu/.
Sur le plan pharmacologique, nous nous intéressons aux propriétés thérapeutiques de la caféine et du ciblage de ses récepteurs cérébraux.
La caféine est la substance psychoactive la plus consommée au monde. Différentes études épidémiologiques, y compris les nôtres, indiquent que sa consommation habituelle/chronique réduit le déclin cognitif au cours du vieillissement mais également le risque développer la maladie d’Alzheimer. Nos études chez l’animal ont permis de fournir, pour la première fois, des bases moléculaires aux effet cognitifs de la caféine favorisant une plasticité épigénomique des cellules neuronales et non-neuronales de l’hippocampe.
L’ensemble de ces travaux ont favorisé un développement translationnel majeur, le projet CAFCA (NCT04570085; https://www.cafca-alzheimer.fr/), un essai clinique de phase 3 vs. placebo randomisé en double aveugle porté par le Pr. Thibaud Lebouvier (CMRR Lille et membre du laboratoire). Nous souhaitons également mieux comprendre les effets moléculaires de la caféine au sein de différentes populations cellulaires en combinant des approches épigénomiques et électrophysiologiques chez l’animal à des études de biomarqueurs épigénétiques plasmatiques chez les patients de notre essai CAFCA.
La caféine est un antagoniste non-sélectif des récepteurs adénosinergiques A2A dont les niveaux en A2AR sont anormalement augmentés, au niveau neuronal et astrocytaire, au cours du vieillissement cérébral et plus encore dans la MA ou d’autres Tauopathies primaires. Dans ce contexte, nous nous intéressons aux conséquences physiopathologiques de la dérégulation neuro-gliale du récepteur A2A sur le plan neuropathoogique et moléculaire. Nous évaluons également leur rôle dans les mécanismes de propagation « prion-like » de la Tauopathie avec l’optique de développer un essai thérapeutique anti-A2A dans le contexte de Tauopathies primaires (Collaborations : Anne-Laurence Boutillier, LNCA, Strasbourg; Christa Müller, Bonn; Annett Halle, DZNE, Bonn; Etienne Audinat, IGF, Montpellier ; Yijuang Chern, IBMS, Taipei, Taiwan ; Sabine Levi, ESPCI, Paris).
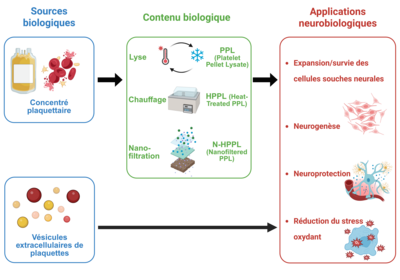
Enfin, en collaboration avec Gregory Kuchcinski, David Devos, Anne-Sophie Rolland (équipe TREAT), et le laboratoire du Pr. Thierry Burnouf à la Taipei Medical University (Taipei, Taiwan), nous développons depuis plusieurs années un projet sur le sécrétome plaquettaire. Ce dernier contient un cocktail synergique de facteurs trophiques, notamment des facteurs de croissance, des cytokines, des molécules anti-inflammatoires et antioxydantes, qui ont le potentiel de favoriser la neurorégénération et la neuroprotection.
Notre objectif est d'étudier de manière préclinique le potentiel thérapeutique de ces préparations plaquettaires dans des modèles murins de Tauopathies par la combinaison d’approches in vivo, moléculaires et en neuroimagerie. Ce projet permettra de fournir de nouvelles informations sur les mécanismes d'action des thérapies dérivées des plaquettes et à développer une biothérapie transférable en clinique.