Tauopathie, interactions neurogliales et neuroimmunes
Personnels impliqués : David Blum, Anna Bogdanova, Luc Buée, Ming-Li Chou, Camille Degryse, Vincent Deramecourt, Marie Dubar, Eloïse Gilbert, Sophie Halliez, Vincent Huin, Brenda Lammens, Thibaut Nicod, Espérance Pastouret, Camille Lefebvre
Dans la maladie d’Alzheimer et les Tauopathies, une perturbation de l’homéostasie neuro-gliale semble prépondérantes dans le développement de la pathologie elle-même mais également de ses conséquences en terme cognitif.
Dans ce contexte, nous cherchons non seulement à mieux comprendre comment la Tauopathie affecte les interactions entre astrocytes et neurones, mais aussi comme ces dysfonctionnements contribuent à la progression de la Tauopathie.
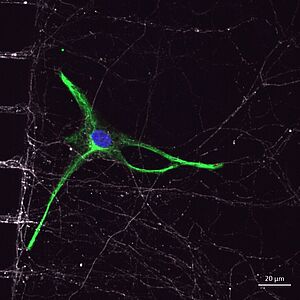
Pour cela, nous réalisons et caractérisons des co-cultures neurones-astrocytes primaires en dispositifs microfluidiques afin d’étudier précisément comment les dysfonctionnements astrocytaires observés dans la maladie d’Alzheimer affectent la transmission synaptique (collaboration avec Alexis Bemelmans & Karine Cambon, MirCen, Fontenay-aux-Roses).
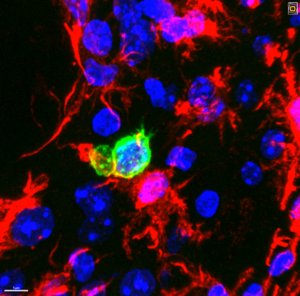
Si la recherche s’est longtemps concentrée sur certaines cellules immunitaires telles que la microglie ou les lymphocytes, notre équipe a choisi d'explorer un terrain encore méconnu : le rôle des neutrophiles et de leurs « pièges extracellulaires » (NET). Nous décryptons comment ces mécanismes sont en lien avec la Tauopathie, influencent la progression pathologique et impacte le paysage neuro-immunitaire et neuro-inflammatoire.
Ces études sont réalisées en combinant l’étude de modèles expérimenTaux innovants et l’analyse de tissus humains autopsique, ouvrant la voie vers de nouvelles stratégies thérapeutiques innovantes (Guillaume Dorothée, CRSA, Paris).
Dans le contexte de ces recherches sur le rôle des interactions neurogliales et neuro-immunes dans la maladie d’Alzheimer et les Tauopathies, nous nous intéressons également à l’impact de certaines infections dans le développement pathophysiologique lié à Tau. Des données épidémiologiques et expérimentales suggèrent en particulier que certaines conditions infectieuses responsables d’une inflammation périphérique chronique de bas grade, comme la parodontite -pathologie inflammatoire chronique des tissus parodontaux induite par une dysbiose bactérienne et communément appelée “déchaussement dentaire”- sont associées à des performances cognitives altérées et à un risque accru de troubles neurocognitifs.
Par ailleurs, le microbiote intestinal, via l’axe intestin–cerveau, est impliqué dans la modulation de la réponse inflammatoire systémique et de processus neurobiologiques pertinents pour les maladies neurodégénératives, incluant la pathologie Tau dans des modèles expérimentaux. Bien que distincts, les microbiotes parodontal et intestinal peuvent contribuer à un contexte inflammatoire systémique commun, susceptible d’influencer certains processus neurobiologiques impliqués dans le déclin cognitif.
Ainsi, nous explorons les associations entre état parodontal, microbiotes oral/ parodontal et intestinal, marqueurs inflammatoires et fonctions cognitives aux stades précoces du déclin cognitif, en combinant approches cliniques, biologiques et précliniques. L’objectif est de mieux caractériser les contextes biologiques associés à la vulnérabilité cognitive précoce, dans une perspective translationnelle (Collaborations : Rodrigue Dessein CHU Lille ; Kathy Dujardin, équipe TREAT).
Par ailleurs, nous nous intéressons également à un agent pathogène neurotrope commun persistant dans le cerveau, Toxoplasma gondii (Tg), qui pourrait donc influencer l’évolution pathophysiologique dans un contexte de Tauopathie.
Nous nous efforçons notamment à identifier et décrypter les mécanismes sous-jacents sur le plan neuronal et neuro-immunitaire (Collaborations : Sabrina Marion, CIIL, Lille ; Elsa Suberbielle & Nicolas Blanchard Infinity, Toulouse)