Nouveaux mécanismes pathogénique de Tau
Personnels impliqués: Séverine Bégard, David Blum, Luc Buée, Léna Chesnais, Vincent Deramecourt, Coraille Fromentin, Sophie Halliez, Brenda Lammens, Camille Lefevbre, Rislane Taouili, Thibaut Nicod, Marie Oosterlynck, Anne Pernodet
L’accumulation de la protéine Tau anormalement phosphorylée, anormalement conformée et agrégée est un événement central dans la maladie d’Alzheimer et les autres Tauopathies. Nous étudions à la fois comment la protéine Tau anormale/pathologique se propage dans le cerveau, contribuant ainsi à la progression de ces maladies, et comment elle favorise la perte synaptique et neuronale. En ce qui concerne la maladie d’Alzheimer, il est maintenant admis que la protéine Tau pathologique se propage dans le cerveau, au moins en partie, via des mécanismes dits « prion-like ». Et c’est sans doute aussi le cas des autres Tauopathies. Cette diffusion de type prion repose sur le transfert d’espèces pathologiques de Tau (« Tau seeds ») d’une cellule atteinte vers une cellule receveuse saine. Une fois internalisées, ces espèces recrutent la protéine Tau physiologique et induisent sa malconformation, aboutissant à la genèse d’agrégats (nucléation ou « seeding »).
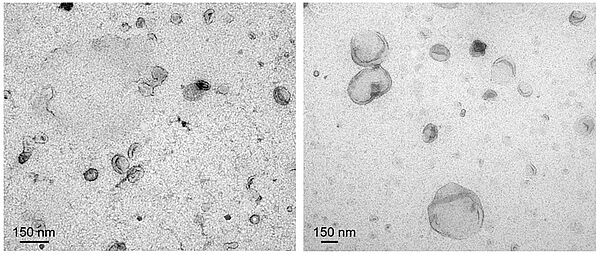
Cette propagation nécessite donc un transfert intercellulaire de Tau pathologique. Notre équipe a montré que ce transfert peut s’effectuer par différents mécanismes: sécrétion de Tau sous forme libre, passage via des nanotubes, ou encore par transport via des vésicules extracellulaires (VE). Récemment, des VE isolées à partir de tissu cérébral de patients atteints de différentes Tauopathies (maladie d’Alzheimer, paralysie supranucléaire progressive et maladie de Pick) ont été étudiées in vitro et in vivo afin d’évaluer leur capacité de nucléation. Ces travaux ont montré que les VE issues de certaines Tauopathies (surtout la maladie d’Alzheimer) contiennent des formes pathologiques de Tau capables d’induire un effet « pro-seeding ».
Dans ce contexte, l’équipe cherche à caractériser en détail les VE d’origine cérébrale humaine, en analysant à la fois leur contenu protéique global et les différentes formes de Tau qu’elles transportent (isoformes, formes clivées, avec ou sans modifications post-traductionnelles). Par ailleurs, une stratification des VE est réalisée afin d’identifier le ou les sous-types vésiculaires responsables de la propagation de Tau. Pour cela, les petites et les grandes VE sont séparées et étudiées distinctement.
Afin d’investiguer plus avant les mécanismes de propagation de la pathologie Tau dans le cerveau et de quelles manières la protéine Tau pathologique perturbe son fonctionnement, nous utilisons des modèles cellulaires et animaux, pour une partie, développés au laboratoire.
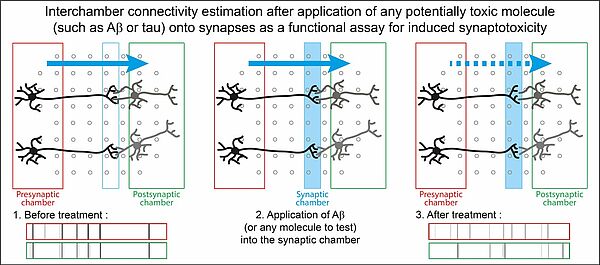
En particulier, nous avons développé en collaboration avec Devrim Kilinc (IPL, Lille), un système cellulaire pour évaluer directement au niveau des synapses la toxicité de molécules (comme les protéines anormales associées à la maladie d’Alzheimer : Aβ et Tau). Dans ce système, des neurones sont mis en culture dans un dispositif microfluidique monté sur une puce à microélectrodes (microelectrode array, MEA). Le dispositif microfluidique est constitué de trois chambres connectées entre elles par de fins microcanaux. Les neurones sont ensemencés dans les deux chambres latérales. Dans ces conditions, les axones émanant de la première chambre et les dendrites émanant de la troisième chambre se rencontrent au sein de la chambre centrale et y forment des synapses. Ces synapses sont fonctionnelles. Ainsi, en comparant l’activité des neurones des deux chambres latérales à partir des enregistrements réalisés au moyen des microélectrodes (MEA), on observe que leurs activités sont synchronisées. Il est alors possible d’appliquer les molécules à tester dans la chambre synaptique dont l’effet est évalué en mesurant l’évolution de la connectivité entre les chambres latérales.
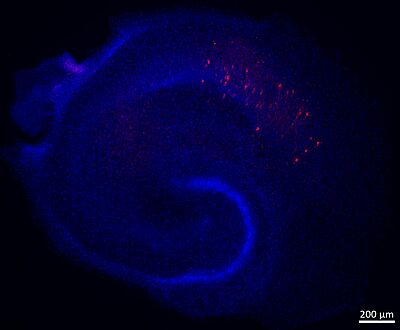
Par ailleurs, nous développons un modèle de Tauopathie potentialisée/induite en culture organotypique hippocampique et adapté aux études par MEA. Ceci dans le but de caractériser les premiers événements moléculaires et cellulaires menant au développement de la pathologie Tau et les conséquences fonctionnelles de celle-ci sur les circuits cérébraux.
Enfin, afin de modéliser de manière pertinente les mécanismes de neurodégénérescence liée à l'âge dans les Tauopathies nous développons en parallèle des modèles cellulaires à partir de fibroblastes reprogrammés soit classiquement en iPSCs, soit en miNs (Neurones induits via des microARNs). Ce dernier modèle est particulièrement intéressant car permet de conserver les marques épigénomiques du donneur, indispensables pour étudier les altérations moléculaires dépendantes du vieillissement.
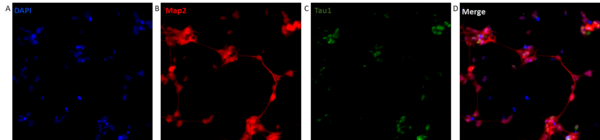
Des fibroblastes humains ont été convertis directement en neurones par activation de microARN neurogéniques transduits par des lentivirus. Les cellules ont été fixées et marquées en immunofluorescence. (A) Marquage nucléaire au DAPI (bleu). (B) Immunomarquage de MAP2 (rouge), indiquant l’identité neuronale et la morphologie dendritique. (C) Immunomarquage de Tau total (vert), révélant l’expression de la protéine Tau dans les neurones induits. (D) Image fusionnée (merge) montrant la co-localisation de MAP2 et Tau dans les cellules converties.
L’ensemble de ces développements méthodologiques nous servent à aborder plusieurs aspects de la pathogénicité de Tau. Notamment, nous avons en particulier identifié une nouvelle espèce de protéine Tau tronquée en N-terminal, AcMet-t11, associée aux enchevêtrements neurofibrillaires aux stades précoces de la maladie d'Alzheimer. Cette nouvelle forme de Tau est produite à partir d'un site d'initiation de traduction alternatif du gène MAPT, un mécanisme non canonique qui n'avait jamais été décrit pour la protéine Tau qui semble lié au déclenchement d’une réponse intégrée au stress (ISR), connue pour activer la traduction alternative. Enfin, nous nous intéressons, in vivo, au lien entre le développement de la Tauopathie, sa propagation et l’émergence de comportement « depression-like » sous l’angle de réseaux dont la dysfonction serait instrumentale dans ces altérations.